Nouveau programme AcSé : l'essai AcSé-HER2
Mis à jour le
Troisième essai clinique mis en place dans le cadre du nouveau programme AcSé lancé avec la Stratégie décennale de lutte contre les cancers. Ouvert aux inclusions depuis le 30 octobre 2025, il est coordonné par Unicancer et financé par l’Institut national du cancer. Le premier patient a été inclus le 17 décembre 2025.
Titre de l'essai : Élargir les options thérapeutiques pour les patients adultes atteints de cancers solides avec une surexpression ou une mutation du gène HER2.
Essai coordonné par le Dr Barbara PISTILLI, Gustave Roussy – Villejuif
Co-coordonnateur : Pr Jean-Philippe METGES, CHU de Brest – Brest
Rationnel de l’essai
Les altérations du gène HER2 sont impliquées dans le processus de développement du cancer. On retrouve ces anomalies à des fréquences très variables (de 2% à 60% environ) dans les cancers du poumon, du sein, de l’estomac, des voies biliaires, des glandes salivaires, du colon, de l’endomètre, de l’utérus, de la vessie, des os, du sang, etc.
Le zanidatamab est un médicament anti-cancéreux agissant sur les cellules avec des altérations du gène HER2. Il est utilisé en Europe pour traiter les personnes atteintes d’un cancer des voies biliaires.
Toutefois, dans le cadre de différents essais cliniques, le zanidatamab a montré une activité intéressante chez quelques patients atteints de différents cancers présentant une altération du gène HER2. Ce traitement pourrait donc être efficace dans plusieurs types de cancers dès lors que l’on détecte une altération de ce gène.
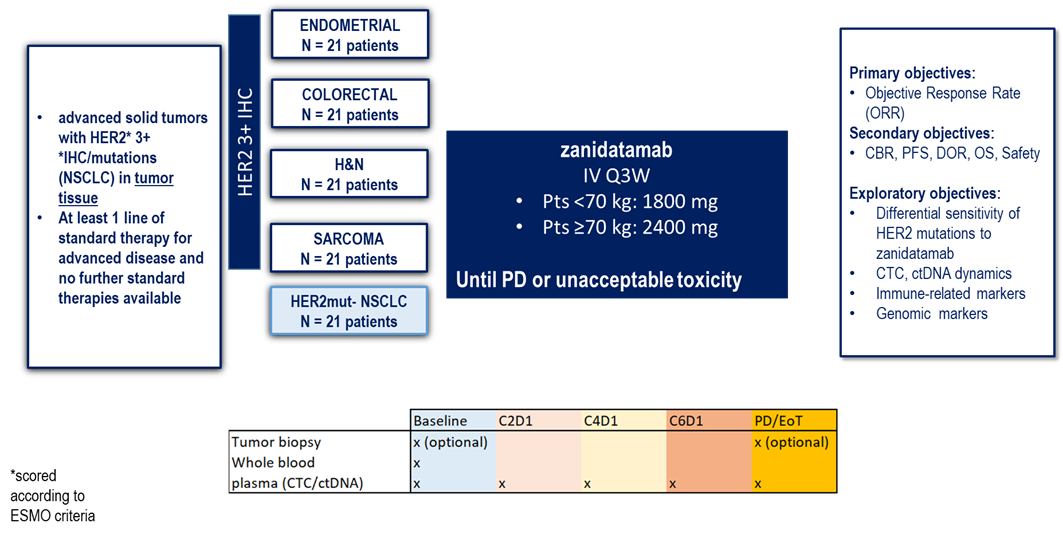
Schéma de l’étude
Objectifs du programme
L’objectif principal est d’évaluer l'efficacité du zanidatamab chez des patients atteints de différents cancers présentant une altération du gène HER2. L’efficacité sera traduite par le nombre de patients chez qui une réduction de taille de la tumeur a été observée.
Des objectifs secondaires porteront sur l’évaluation de l’efficacité mesurée sous d’autres formes comme la durée de la réponse observée sous traitement, l’impact sur le délai de survenue d’une nouvelle progression et la survie globale. L’essai clinique évaluera également la sécurité du zanidatamab.
Pathologies concernées :
- cancer de l’endomètre ;
- cancer colorectal ;
- cancer de la tête et du cou ;
- sarcome ;
- cancer du poumon.
État d’avancement du programme au 18 décembre 2025
- 4 centres ouverts activés/20 centres participants : liste des centres actifs
Liens utiles :